Обе эти вакцины, хоть и предназначены для защиты от COVID-19, созданы с использованием разных технологий.
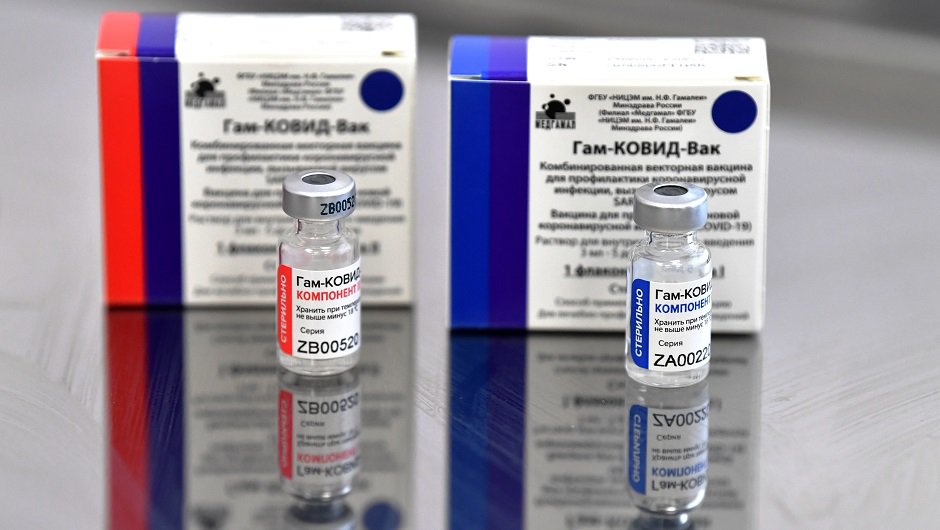
В основе вакцины Спутник V — человеческий аденовирус, который используется как переносчик генетической информации вируса SARS-CoV-2. После его попадания в организм в клетках начинается синтез и сборка вирусного S-белка. Именно из этого белка и состоят те самые, напоминающие корону, шипы на поверхности вируса, из-за которых вирус и получил свое название. Образование S-белка провоцирует развитие иммунного ответа, в организме синтезируются антитела, обеспечивающие защиту от вируса.
Информация о I и II фазах клинических испытаний этой вакцины, в которых изучается безопасность препарата и подбирается доза вакцины, опубликована в авторитетном научном журнале The Lancet. О серьезных побочных эффектах, связанных с введением вакцины, не сообщается.
Прививаться Спутником нужно в два этапа с перерывом в три недели. Вакцина двухкомпонентная, на первом и втором этапах в качестве вектора используются разные аденовирусы: сперва более редкий аденовирус-26, а потом более распространенный аденовирус-5.
Все дело в том, что аденовирусы могут и сами по себе вызывать разные заболевания и провоцировать формирование иммунного ответа. Векторный аденовирус может быть воспринят как «враг», который будет атаковаться антителами против него — из-за этого прививка может оказаться неэффективной. Чтобы снизить вероятность такого исхода, и используется двухэтапная вакцинация с применением аденовируса-26, вероятность контакта с которым в прошлом довольно мала. По оценкам производителей, эффективность вакцины Спутник V составляет около 92%.
Источник: Пресс-служба Роспотребнадзора
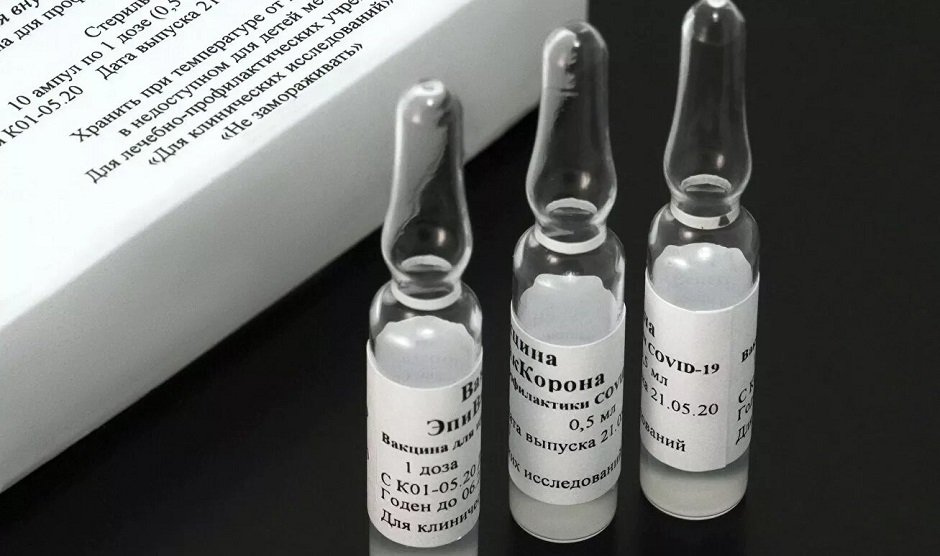
ЭпиВакКорона сделана специалистами из новосибирского центра «Вектор» по иной технологии. Это пептидная вакцина, которая состоит из трех пептидов — коротких последовательностей аминокислот, соединенных с белком-носителем и адъювантом. Введение вакцины приводит к синтезу небольших фрагментов вирусных белков, которые и должны провоцировать формирование иммунного ответа.
В открытых источниках информация о результатах доклинических (без участия людей) испытаний отсутствует. Данные о I и II фазе клинических испытаний представлены очень скудно — известно лишь о числе участников — 14 и 86 человек соответственно, а также о том, что «индукция специфических антител произошла у 100% добровольцев». III фаза клинических испытаний проводится только сейчас, уже после регистрации препарата. Известно, что побочных эффектов у 1438 добровольцев, получивших дозу вакцины, выявлено не было.